CONTENTS
INTRODUCTION
イントロダクションBEGINNING
生命現象を解き明かす鍵、「糖鎖」BREAKTHROUGH
プロジェクトの突破口FOR THE FUTURE
技術をビジネスにつなげ世界スタンダードを目指す
FACE
大胆な発想と地道な努力INTRODUCTION 概要
生命現象に深く関与する糖鎖。 複雑な構造を解析する強力なツールが誕生しました。
BIGINNING 開発への道
生命現象を解き明かす鍵、「糖鎖」
2003年、生命の設計図ともいえるヒトゲノムが解読されました。しかし、ゲノム情報は4つの塩基で表された文字列にすぎません。
生命現象を解き明かすには、この文字列から、どんなタンパク質がつくられ、どのように機能するのか、詳しく調べる必要があります。そんなポストゲノム研究が盛んな中、タンパク質の働きに深く関与する「糖鎖」が、核酸、タンパク質に次ぐ、第3の生命鎖として注目をあつめています。
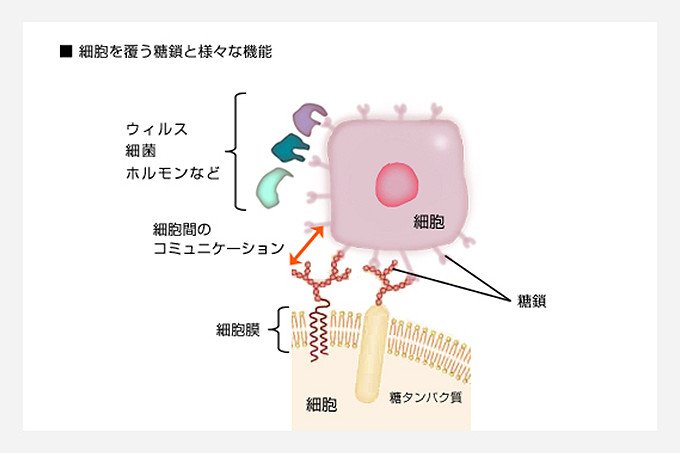
糖鎖は細胞膜に埋まったタンパク質や脂質に結合し、細胞表面を被っています。「細胞の顔」とも呼ばれ、体内の情報伝達を調整しながら、増殖や分化といった細胞活動に影響を与えています。ガンをはじめとする多くの疾患や、免疫機構、ウイルス感染に、深く関与しているので、生体の状態を知る重要な指標になると期待されています。
例えば、ガン細胞では通常の細胞とは異なる特殊な糖鎖が現れることがあります。このように、疾患による糖鎖の変化を発見できれば、これを目印(バイオマーカー)として、病巣の早期発見や適切な診断に利用することができます。
また、糖鎖によって薬の作用メカニズムを制御し、薬効を高めることはもちろん、糖鎖をターゲットにして新薬の開発をすることもできるでしょう。
糖鎖の特徴を抽出する糖鎖プロファイリング
糖鎖には医療を向上する様々な応用が期待されます。これを実現するためには、糖鎖構造を解析し、生命現象との対応を明らかにしていかなくてはいけません。しかし、糖鎖は、核酸やタンパク質に比べ、格段に複雑な構造をもちます。
糖鎖は、グルコースやガラクトースといった単糖類が鎖のようにつながった物質です。直鎖構造ではなく枝分かれをした樹状構造で、組み合わせのバリエーションも豊富なため、潜在的な多様性があります。糖鎖の構造解析には、質量分析装置や液体クロマトグラフィーを用いますが、このように多様性に富む構造を決定するのは至難の業です。時間がかかる上、分析に用いる検体量も必要になります。
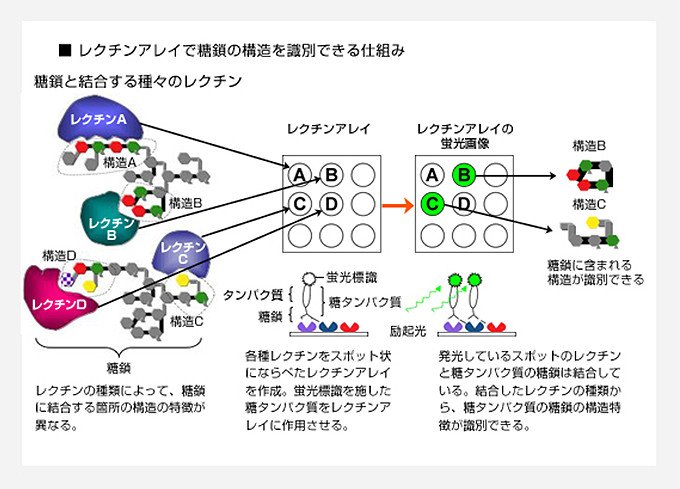
そこで、糖鎖構造を完全に解析するのではなく、部分的な特徴、即ち生物学的に意味のある特徴的なエピトープ構造を抽出する、糖鎖プロファイリングという手法が検討されています。その中でも、レクチンを利用した斬新なアイディアを提唱しているのが、産業技術総合研究所糖鎖医工学研究センターの平林淳副センター長のチームです。
レクチンは糖鎖に親和性をもつタンパク質の総称で、ヒトからウイルスまで生物界に広く分布しています。平林副センター長らは、レクチンの種類によって、糖鎖に結合する箇所の構造の特徴(分岐度や結合様式、末端修飾の有無)が異なることに注目しました。糖鎖に結合するレクチンの種類から、糖鎖にどのような構造の特徴があるのか識別できると考えたのです。即ち、目的によっては、糖鎖構造をディジタル的に完全に同定する必要などなく、レクチンが捕まえている情報をうまく使えれば、それで十分だと割り切った訳です。
平林副センター長らは、まず100種類以上のレクチンと糖鎖の間の親和性について調べました。その中から45種類のレクチンを厳選し、スポット状に並べて固定したレクチンアレイを開発しました。生体内の糖鎖はタンパク質や脂質に結合し、糖タンパク質や糖脂質として存在しています。
そこで糖タンパク質に蛍光標識を施し、レクチンアレイと相互作用させれば、糖鎖が結合しているレクチンのスポットだけが発光します。このレクチンアレイの蛍光画像から、どのスポットが、どのくらい発光しているのか解析すれば、糖タンパク質に含まれる糖鎖の構造の特徴と、その特徴をもつ度合いが、識別できるはずです。
しかし、レクチンアレイの蛍光画像を取得するには難しい問題がありました。当時使われていた装置では、試料(アレイ)を洗い流す工程が必要でした。しかし、レクチンと糖鎖の結合力はとても弱く、洗浄すると糖タンパク質が剥がれてしまいます。これでは、正確な結果が得られません。
改良を積み重ね製品化
そこで平林副センター長は、現在、株式会社GPバイオサイエンス(当時、株式会社モリテックス・グライコミクス研究所長)の取締役である山田雅雄さんらが、日本レーザー電子株式会社で開発を手がけたSCANⅢに目をつけました。
SCANⅢは世界で唯一、試料を洗浄せず、液相のままアレイの蛍光画像を撮影できる装置でした。2002年暮れ、平林副センター長から誘われNEDOプロジェクトに参加した山田さんは、レクチンアレイの蛍光画像から糖鎖構造を分析する、糖鎖プロファイラーの開発に着手しました。
レクチンアレイを用いれば、糖鎖の構造の変化は、スポットの発光パターンや発光強度の変化として検出されます。このため、レクチンアレイの蛍光を正確に検出し、画像を取得することが、技術の要となります。
山田さんは「開発は、細かなチューニング作業の積み重ねだった」と語ります。開発当初は、蛍光が全く検出されなかったり、同じレクチンアレイを測定しているにも関わらず分析結果が異なったりと、よい結果がだせませんでした。
しかし、カメラの選定、熱の対策、励起光フィルターと検出光フィルターの波長域や帯域幅の調整、スライドガラスの工夫、レクチンの固定化法など、試行錯誤を繰り返しながら、根気強くシステムの最適化をはかりました。その結果、SN比(検出信号とノイズの比)を100倍以上改善し、安定的にレクチンアレイの蛍光画像を分析できる装置が完成したのです。そして遂に2006年10月、糖鎖プロファイラーが製品化され、販売が開始されました。
現在でも、装置の改良は続いています。装置のハード面を担当している齋藤敦さんは、「感度を今より一桁上げて、見落としていたかもしれないバイオマーカーを検出したい」といいます。一方、試料や検体の操作を担当する武石俊作さんは「新しいバイオマーカーをみつけ、疾病の診断キットを開発したい」と語り、新しいアプリケーションを開発する重要性を強調します。

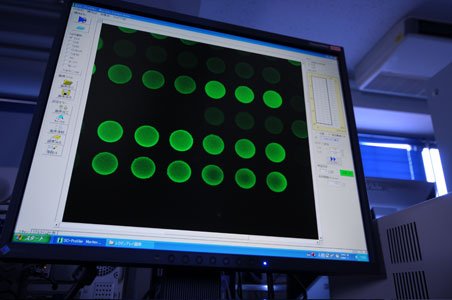
糖鎖プロファイラーにレクチンアレイをセットする様子
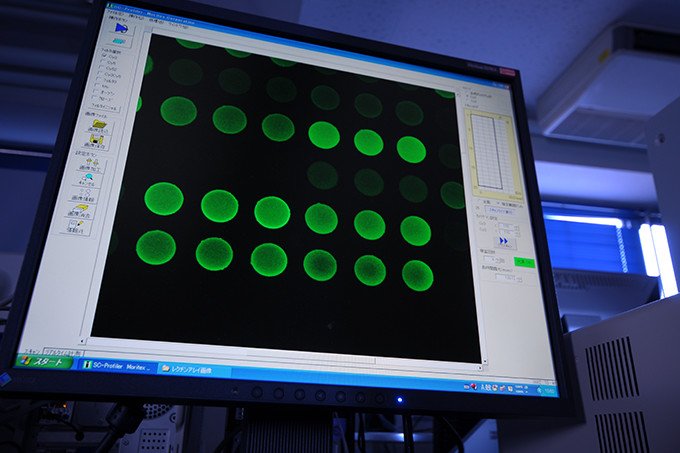
糖鎖プロファイラーで取得されるレクチンアレイの蛍光イメージ

装置の状態を確認する、齋藤敦さん
BREAKTHROUGH プロジェクトの突破口
レクチンアレイの蛍光画像を高精度に取得するには、SCANⅢで培ったエバネッセント場を蛍光色素の励起に利用する技術が欠かせません。
通常、DNAアレイなどの蛍光画像を撮影する装置では、スライドガラスの上、或いは下からアレイにレーザーなどを光源として励起光を集光照射し、アレイに捉えられた物質に標識された蛍光色素を発光させます。このため、蛍光標識された物質が浮遊する液相を残したままだと、アレイの液層全体が発光してしまい、SN比が下がってしまうのです(右図)。
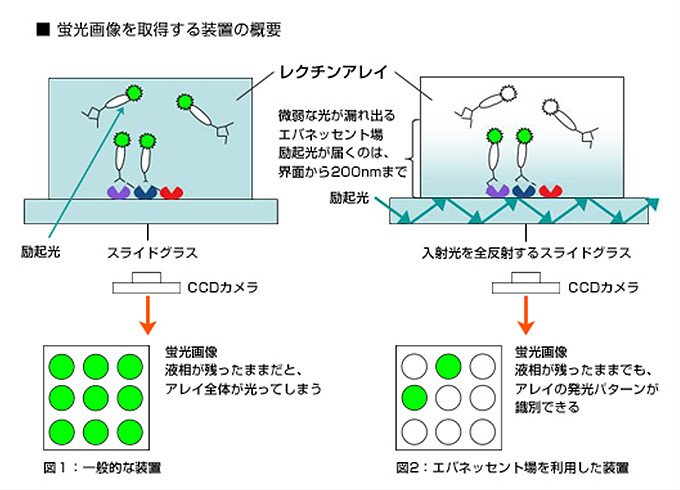
しかし、レクチンアレイは、糖鎖との結合力が弱く洗浄できないので、余分な液相を取り除くことができません。そこで、レクチンアレイがスライドガラスと接する界面付近だけを発光させようと考えました。
エバネッセント場とは、光を全反射するガラス表面から微弱な光が染みでる状態のことを指します。ガラス表面を離れると光の強さが指数関数的に急激に弱まります。
蛍光色素を励起できる強度の光が届くのは、界面から100nm~200nm程度です。レクチンと結合している糖鎖が存在するのも、ちょうど界面から100nm~200nm程度。そこで、全反射するスライドガラスに光を照射してエバネッセント場を発生させると、レクチンアレイに結合する糖タンパク質だけを発光できました。
この技術を利用して、洗浄をせずに液相を残したまま、レクチンアレイの蛍光画像を取得することに成功しました。
FOR THE FUTURE 開発のいま、そして未来
技術をビジネスにつなげ世界スタンダードを目指す
解析手法が未発達であった糖鎖は、これまで研究が難しいと考えられてきました。しかし、糖鎖プロファイラーを使えば、少ない量の検体から、簡単な前処理で、短時間ではっきりと構造の特徴を抽出することができます。多数の検体を比べ、速やかに糖鎖構造の違いを見つけ出せるので、バイオマーカーを探し当てる強力なツールとなると期待されます。

エバネッセント波蛍光励起法による糖鎖プロファイラー GlycoStation Reader 1200
また、最近では、糖鎖が幹細胞の分化能の保有状態や分化方向の同定に有効であることが明らかになり、山田さんらは、産総研の協力の下、国立成育医療センターの梅澤先生、阿久津先生らとともに、再生医療の現場で使用する糖鎖プロファイラーとレクチンアレイの開発を進めています。
山田さんは「糖鎖研究に対するNEDOの長期的なサポートが実を結んだ、世界でも他に例をみない装置です。この装置を糖鎖研究の一般的なツール、インフラとして確立していきたい」と、糖鎖プロファイラーにかける熱い思いを語ります。
製品化の際、糖鎖プロファイラーの将来性を確信した山田さんは、バイオで成功するには、デファクトスタンダードのポジションを掴むべきだと考え、発売当初から世界を舞台にビジネスを展開すべきとの信念から、国内のみならず、海外まで、自ら営業活動を行いました。
しかし、営業先としてバイオ・医療業界に特別なコネクションがあったわけではありません、ましてや山田さんは元々が半導体屋さんでした。展示会や学会を利用して、地道に顧客を開拓していきました。「現在、引き合いの80%は海外です」と山田さん。糖鎖プロファイラーを日本発の世界のスタンダードにするべく、技術とビジネスの両面から、全力で取り組んでいます。(2009年2月取材)
開発者の横顔
大胆な発想と地道な努力
山田さんと武石さんは、以前、同じ電子機器メーカーで、半導体を開発していました。
山田さんがバイオ分野への転身を決意したきっかけは、開発に対する強い思いからでした。「プロジェクトリーダーとして世界トップクラスの130nm(110nm)の半導体技術を開発したものの、なかなかお客様が付きません。資金を投じて技術を開発しても使ってもらえなければ意味がないと思い、自分で事業企画をたて、そのなかで技術開発をしたいと考えるようになりました」。
しかし半導体の開発には巨額の資金が必要です。そこで小規模な投資でも開発ができる、バイオ分野に目をつけ、ベンチャー企業に転職しました。その後、株式会社モリテックスに異動し、グライコミクス研究所を立ち上げ、集中的に糖鎖プロファイラーの開発を進めました。山田さんは「お客さんの声を自分の事業戦略に落としこみながら開発するのは、本当に面白い」と語ります。
一方、武石さんのきっかけは、生命に対する学問的な興味でした。「物理学を専攻していた学生時代から、"生命と何か"という謎に興味を持ち続けていました」。入社後もその思いは消えず、社会人学生としてタンパク質の構造解析を研究し、博士号を取得しました。
山田さんから糖鎖プロファイラーの話を聞き、糖鎖の将来性が十分理解できたので、上市直前の2006年2月から、開発メンバーに加わりました。
分野を超えて挑戦する二人の出会いが、糖鎖プロファイラーの開発を支えています。

株式会社GPバイオサイエンス
山田さん

株式会社GPバイオサイエンス
武石さん
お読みいただきありがとうございました。
ぜひともアンケートにお答えいただき、
お読みいただいた感想をお聞かせください。
いただいた感想は、
今後の連載の参考とさせていただきます。