
CONTENTS
INTRODUCTION
安全性が高く、コストも安いと期待、再生治療の産業化に向けて成果が着実に
BEGINNING
軟骨の損傷や摩耗による、ひざの痛みを抱えている人には、
福音となると期待して開発をスタート
BREAKTHROUGH
無血清培地の材料選定に悪戦苦闘FOR THE FUTURE
製薬企業とライセンス契約し、患者のQOL向上を目指す
FACE
再生医療が新しい産業になるINTRODUCTION 概要
安全性が高く、コストも安いと期待、再生治療の産業化に向けて成果が着実に
変形性膝関節症や外傷性軟骨損傷、離断性骨軟骨炎など、軟骨の損傷や摩耗を伴う疾患は、予備軍も含めて国内罹患者がとても多いと言われています。損傷した軟骨は自力で再生することはできず、変形性膝関節症では重症化すると、人工関節を手術で埋め込むしかなく、根治が難しい疾患です。広島大学発のベンチャー企業である、株式会社ツーセルや株式会社スペース・バイオ・ラボラトリーズ、大阪大学、大阪保健医療大学、広島大学などは共同でNEDOプロジェクトに参画し、再生治療の産業化を目指しました。そして、そこで得られた画期的な成果の一つが、いよいよ膝関節の外傷性軟骨損傷および離断性骨軟骨炎を適応疾患の罹患者を対象とした、臨床試験の段階まで到達しました。
BIGINNING 開発への道
軟骨の損傷や摩耗によるひざの痛みを抱えている人には、福音となると期待して開発をスタート
超高齢化社会を迎える日本にとって、ひざの痛みや変形など、ひざ軟骨の損傷による疾患は大きな社会問題となってきています。高齢者の中には、歩行がつらいことを理由に外出の機会を減らし、そのうち家に閉じこもりがちになり、健康を損なう場合も少なくないからです。
ひざ軟骨の疾患は、初期であれば湿布や痛み止めなどでの治療も可能ですが、軟骨はいったん損なうと自己再生することがありません。ひざ軟骨の疾患の一つである変形性膝関節症(罹患者数は予備軍を含め国内で3,000万人と推定され、国民病と言えるほど)では、重症化すると、骨端を切除して人工関節を埋め込むしか治療方法がありません。
(出典:厚生労働省「介護予防の推進に向けた運動器疾患対策に関する検討会『介護予防の推進に向けた運動器疾患対策について 報告書』」 (2008))
つまり、軟骨の損傷による関節疾患は根治が難しく、患者への負担が大きい疾患だと言えます。
そうした中で、広島大学発のベンチャー企業である株式会社ツーセルを中心に、同じ広島大学発ベンチャー企業の株式会社スペース・バイオ・ラボラトリーズ(SBL)、大阪大学、大阪保健医療大学、広島大学などは、NEDOの「ヒト幹細胞産業応用促進基盤技術開発」プロジェクト他を通じ、再生医療の産業化に役立つ技術として、「滑膜由来間葉系幹細胞培養技術」と「模擬微小重力環境での大量培養技術」を開発しました。
そして、その技術をもとに膝軟骨再生細胞治療製品「gMSC®1」(臨床試験中)や重力を制御できる世界初の培養装置「Gravite®(グラビテ)」が生まれました。
基礎研究を経て、NEDOの支援で産業化を目指す
「滑膜由来間葉系幹細胞培養技術」の開発の端緒は、ツーセルの創業者である辻紘一郎同社社長、加藤幸夫同社取締役副社長(広島大学名誉教授)の出会いにありました。
中外製薬株式会社で長らく開発に従事していた辻社長は、在職中だった20年ほど前に、アメリカの学会で加藤副社長(当時は広島大学教授)と同席する機会がたびたびあり、互いに親交を深めていったと言います。
加藤副社長は当時、広島大学で軟骨細胞の分化や細胞培養の研究をしていました。2000年に他の公的機関のプロジェクトに参画した際、加藤副社長が辻社長に声をかけ、辻社長も翌年に同プロジェクトに参画。その中で2人が着目していたのが間葉系幹細胞(MSC=Mesenchymal Stem Cell)です。
MSCは骨や軟骨、脂肪、筋肉、神経などに分化する力を持った幹細胞で、人の全身に幅広く存在します。特に滑膜組織から採取されたMSCには、高い増殖能力があり、軟骨再生に大きな力を発揮すると期待されています。プロジェクトでは、2人はMSCの培養・超増幅技術の確立を目指しました(図1)。
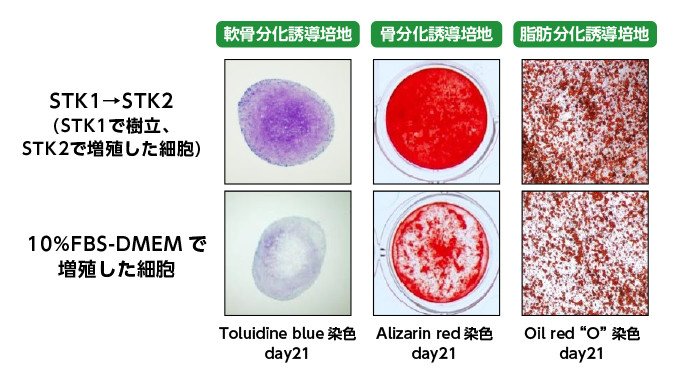
図1 ヒト滑膜組織由来MSCの軟骨・骨・脂肪への分化の様子。ツーセル開発のMSC用無血清培地「STK®シリーズ」を用いた場合(上段)。従来の有血清培地を用いた場合(下段)と比較して軟骨・骨への分化能力が高い (画像提供:ツーセル)
3年間の研究の末、MSCの培養・超増幅技術を確立し、その成果を製品化するために、2003年に辻社長と加藤副社長の2人で、広島大学発のベンチャーとしてツーセルを設立しました。
2004年、資金もない中で、2人と邵金昌同社研究本部長(当時 独立行政法人科学技術振興機構(JST)研究成果活用プラザ広島研究員)が取り組んだのが、MSC用の「無血清培地」の開発でした。
通常、幹細胞の培養ではその細胞増殖を促進させるために、ウシなど動物由来の血清を培地に添加します。しかし、そうした血清を用いることには三つの問題がありました。
まず、培養細胞の品質が安定しないという問題です。次に、血清に潜むウイルスやプリオンなどによる感染やアレルギーのリスクがあるという安全性の問題です。そして、血清を添加しても、幹細胞の種類や個体差によっては、細胞が増殖しないなどの問題があり、これらは血清の組成の影響によるものです。
当時は世界の誰も無血清培地の開発に成功していない中、3人は、単に無血清であるだけではなく、従来よりも高品質のMSCを得ることを培地開発の目標としていました。邵研究本部長が中心となって試行錯誤の末、無血清培地の開発・改良を行い、2008年に世界初のMSC用無血清培地「STK®2」を発売。2010年に「STK®1」が発売開始となりました(図2)。
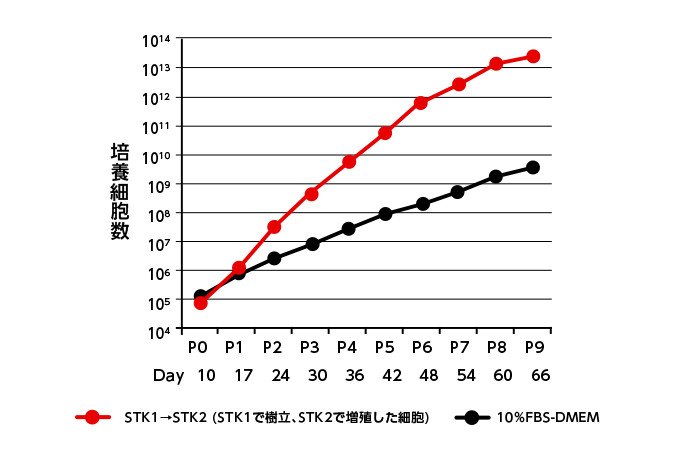
図2 従来の血清培地(黒)と、STK®1・STK®2(赤)の増殖曲線の違い。縦軸が細胞数、横軸が継代数(P)および培養期間を表す (資料提供:ツーセル)
「STK®2」が継代培養(培養組織や培養細胞を別の培養容器に植え継いで培養する)用で、「STK®1」が初代培養(生物から採取した組織や細胞を最初に培養容器で培養する)用です。「STK®1」に続き、同じ2010年には、骨分化用の無血清培地である「STK®3」も発売開始となりました(写真1)。
写真1 無血清培地「STK®2」(左)と、そのシリーズ(右)
このように世界初の画期的な無血清培地を開発したものの、それは、辻社長と加藤副社長にとって準備段階でしかありませんでした。これをベースに軟骨損傷に対する再生医療という重いドアを押し開くことを決意していました。
辻社長は、「他の公的機関から受けた支援はあくまでも基礎的な研究の支援でした。再生医療の産業化を目指す上では、NEDOの支援を仰ぐ他はないと、加藤副社長と話し合いました。私自身、過去にもNEDOプロジェクトに関わり、サブリーダーとして企業などをまとめてきた経験もあり、NEDOならば無血清培地の開発を評価してくれると思ったのです」と語ります。
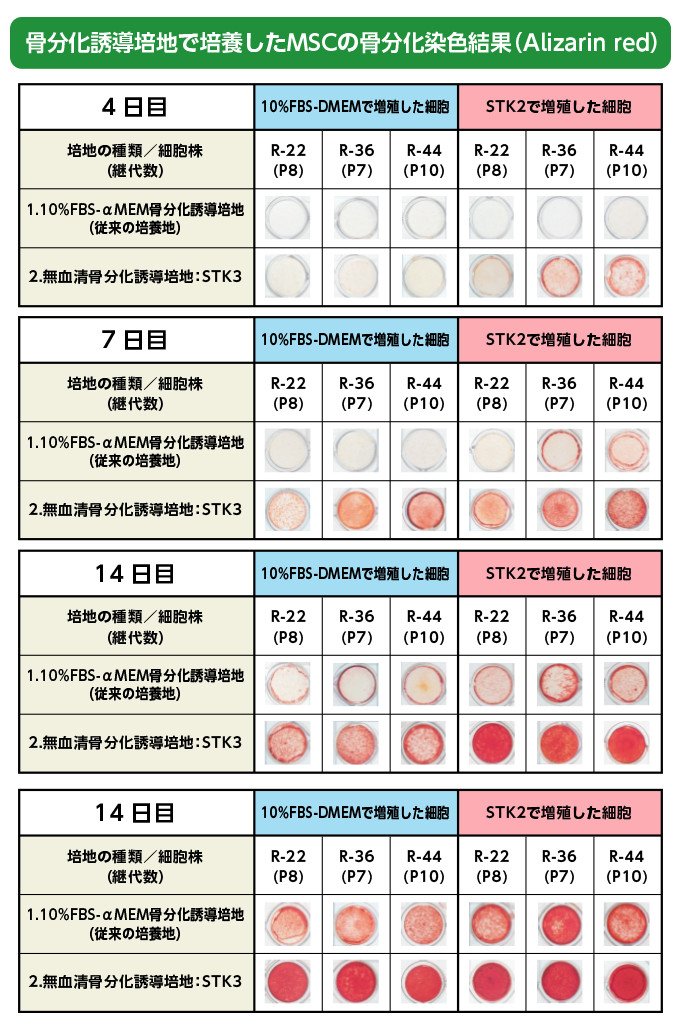
図3 ヒトMSCの骨分化に及ぼす血清培地と無血清培地(STK®3)の影響比較。左側が従来の有血清培地を用いた場合、右側が「STK®シリーズ」を用いた場合 (資料提供:ツーセル)
3次元人工組織(TEC)と無血清培地のマッチング
辻社長と加藤副社長がアメリカで出会った同じ頃、今回の成果で重要な役割を果たした、大阪大学国際医工情報センターの中村憲正教授も、アメリカに留学していました。再生医療の産業化という夢を抱く辻社長は、中村教授とも意気投合し、以降3人の長い付き合いが始まりました。
そして、再生治療の産業化を目指すきっかけとなったのが、中村教授が開発した「スキャフォールドフリー3次元人工組織(TEC=Tissue Engineered Construct)」でした。
幹細胞を増殖・分化させるには、生物由来材料や高分子化合物を使った足場(スキャフォールド)を使うことが一般的ですが、中村教授は「長期にわたるスキャフォールドの体内使用には、その安全性が不明である」という課題があると考えました。
その課題を解決すべく、中村教授らの研究グループでは、2004年からスキャフォールドが不要で、細胞自身が3次元のマトリックス構造を持つ人工組織である「TEC」の開発をスタートしました。
2006年にはNEDOの「再生医療評価研究開発事業」に参画し、「TEC」を用いた軟骨再生エレメント構造体作製に取り組みました。
しかし、「TEC」の産業化を見据えて開発を進めていた中村教授にとって、一つ大きなハードルがありました。それは、培地として有血清培地を用いていたことです。先にも述べた通り、血清を用いることには産業化の上で問題があったのです。
そこで、ツーセルがMSC用無血清培地を開発したことを知った中村教授は、試験的にその培地を滑膜由来のMSCに使用してみました。
両者の相性が適合するか懸念はありましたが、滑膜由来MSCに無血清培地は高度に適合しました(図4)。
その結果を受け、滑膜由来MSCや「TEC」の産業化の可能性を感じた中村教授は、2010年よりツーセル他と共同で、NEDOプロジェクト「ヒト幹細胞産業応用促進基盤技術開発」に参画し、ツーセルのMSC用無血清培地を使って滑膜由来MSCの大量培養の研究を推進しました。
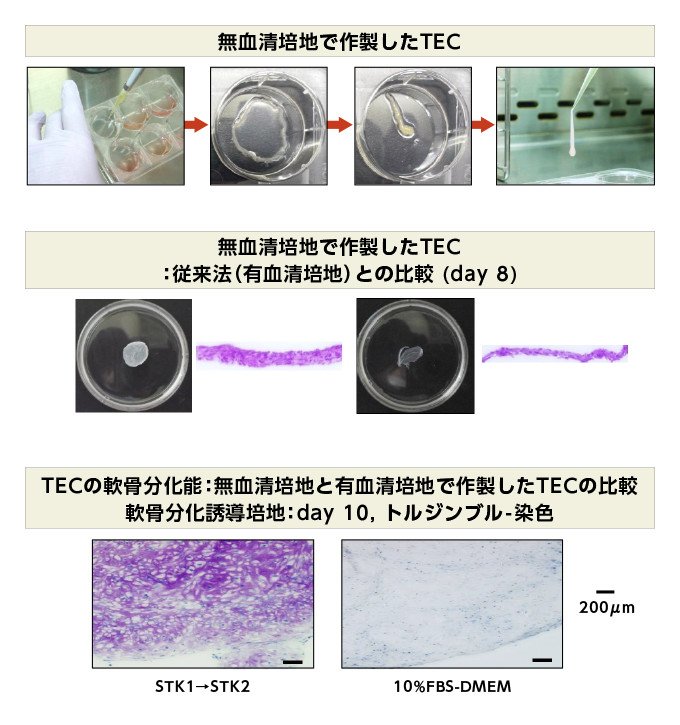
図4 (上段)無血清培地での「TEC」作製の様子。左から3番目までが培養容器から「TEC」を回収する作業。右が完成品 「TEC」。(中段)有血清培地との形態学(4%PFA固定後)及び組織学的(H.E染色)比較。左が無血清培地、右が有血清培地を使用した場合。(下段)有血清培地との軟骨分化能力比較。左が無血清培地、右が有血清培地を使用した場合 (資料提供:ツーセル)
BREAKTHROUGH プロジェクトの突破口
無血清培地の材料選定に悪戦苦闘
無血清培地の開発に加え、ツーセルでは、1人から採取した細胞で複数人分の培養ができる「他家(たか)移植」にも取り組みました。
これまで細胞の移植などによる治療では、患者自身の細胞を採取し、培養して移植する「自家(じか)移植」が一般的でした。しかし、自家移植では一度に1人分の製剤しか作製できない、という問題がありました。
加藤副社長は、他家移植の重要性をこう指摘します。「自家移植では、細胞の採取から培養まで数カ月かかり、コストも高くなります。一方、他家移植は、培養が2週間から1カ月ですみ、大量に低コストで生産し、しかもすぐに病院で使えるので、再生医療の産業化には不可欠な方法と言えます」
しかし、他家移植を採用したことは、開発スタッフにとって大きなプレッシャーでした。
開発の中心的な役割を担ったのは邵研究本部長と長谷川森一研究本部副本部長(兼gMSC®センター長)でした。長谷川さんは、「私は入社7年目ですが、入社当時、他家移植には懐疑的でした。他家移植では拒絶反応が強いため、実現は難しいと思ったのです」と言います。
「加藤副社長や邵研究本部長は、無血清培地をゼロから開発した方ですので、知識量が私たちとは格段に違うのです。それに追いつくのが大変で、9カ月ほど経ってからようやく無血清培地の扱い方が分かりました」(長谷川さん)
臨床(他家移植)に用いる培地として最適な組成にすることを目的に、研究を進めていましたが、材料の種類も多く、それぞれについて異物が混入していないかなど、安全性を確保しなければなりません。材料は免疫に関係するタンパク質である「サイトカイン」や、同じくタンパク質の「アルブミン」などを使います(図5)。

図5 各種遺伝子組み換えヒトアルブミン(①~④、計4種類)を用いて連続継代培養細胞の写真(P2~P4:2代目~4代目の細胞)(資料提供:ツーセル)
長谷川さんは、「体内に入れるものを製造する培地ですから、材料の採取先から加工までトレースできるクオリティの高い材料に変更していきました」と話します。
「しかし、調達先が国内にはなく、海外から購入するしかなかったのですが、調べていくと、その大本となる原料メーカーは一つのベンチャー企業でした。その品質証明がなかなか取れずに、確認できるまで相当な時間を割くことになりました」(長谷川さん)
調査先は欧米から中国、中東にまでおよび、サンプルを取り寄せるのに船便で送ってくるため2〜3カ月かかることもありました。しかも、材料はタンパク質なので熱で性質が変化してしまうときもあり、再度取り寄せるなど、さらに時間がかかりました。
受け取ったサンプルが培地として使えるか調べ、組成比率を変えて実験を繰り返しました。こうした作業に3年ほど費やし、最終的には11種類の材料を入れ替えて最適な無血清培地を作り上げました。
3年かけて80人のドナーの滑膜組織から培養実験を繰り返す
こうした培地作りと並行して、「ヒト幹細胞産業応用促進基盤技術開発」プロジェクトでは、滑膜由来MSCの増殖実験が行われました。
この工程は、どの患者(ドナー)の組織でも常に変わらない高品質のMSCを培養できることを証明するために行うもので、他家移植には必須でした。中村教授が、実験に同意してもらったドナーから滑膜組織を採取し、それをツーセルに送って、MSCの培養実験を繰り返しました。
そして、2010年から3年かけて合計80人の患者の滑膜組織を培養し、無血清培地と有血清培地での比較も行いながら、さらに実験を繰り返しました。
長谷川さんは、「中村教授から送られてくる滑膜組織をシャーレに蒔いて培養します。ツーセルでは骨髄由来のMSCも実験していましたが、滑膜由来MSCの方が早くて元気がいいので、まるで植物の芽が日に日に伸びていくような感じでした」と振り返ります(図6)。
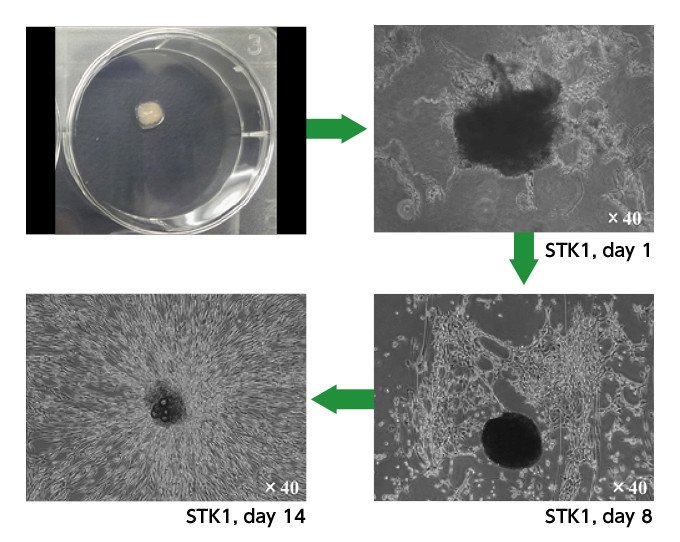
図6 滑膜組織の無血清培地によるMSC分離・初期培養。左上が滑膜組織をシャーレに蒔いた状態。その後、1日目(右上)、8日目(右下)、14日目(左下)の培養状況 (資料提供:ツーセル)
実用化に向けて苦難を乗り越え大量培養のための「gMSC®センター」を開設
こうした土台となる実験が終わり、ツーセルは、無血清培地で滑膜由来他家MSCを培養して「TEC」を活用し、膝軟骨再生細胞治療製品のプロトタイプ製剤を完成させ「gMSC®1」と名付けました。
ツーセルは、さらに2014年からは、NEDOプロジェクト「イノベーション実用化ベンチャー支援事業」に参画し、「gMSC®1」の実用化で必要となる製剤化技術の開発に取り組みました。
その中で、「gMSC®1」の大量培養の実証実験を行うための施設として、「gMSC®センター」を新設しました。
再生医療製品は生きた細胞を製品とするため、製剤化後の滅菌処理が行えません。そのため、「gMSC®センター」は、無菌環境の中での滑膜組織の受け入れ・細胞培養・製剤化・パッケージング・出荷までの、工場にあるような一連の再生医療製品の生産工程を備えた施設として設置されました(写真2)。
製品の品質保証を担当する岩本佳央梨副センター長は、「『gMSC®センター』は、量産工場になぞらえて作られていますが、当時の体制は実証実験段階以上のものではありませんでした。培養作業だけでなく、記録や確認、承認などすべて自分たちで行います。大量培養の実験とは言え、限られた人数で対応しなければならず、苦労の連続です。しかし、この施設での実証実験で、今後に向けて何が足りなくて、何が必要か、それが分かったことは重要なことでした」と語ります。

写真2 (左)gMSC®センターへの入室にはセキュリティカードが必要。(右)センター内の様子が外部から分かるよう、見学用の窓を設置
「短期では成果の出ない地道な実験をNEDOが評価してくれました」
松本昌也治験推進室副室長は、当時の状況をこう語ります。「有血清培養では時間がかかる一方、無血清培養では時間も早く、品質も安定していることは分かっていましたが、実用化レベルでの大量培養となると、従来のラボレベルの量では見えていなかったいろいろな課題が出てきました」
実用化レベルでの大量培養では、生産量がラボレベルの10〜100倍にもなります。そのため作業時間が長くなり、細胞に与える影響も違ってきます。ラボレベルと同じことをやっていても結果が違ってしまうこともあり、その原因を追及して改善を繰り返すしかありませんでした。
松本さんは、「なにしろラボレベルでは起こったことがないことが起きるし、ミスも発生します。例えば継代培養では、細胞をはがすときに剥離剤を使いますが、大量培養での剥離剤の適切な量が分からず、突然、細胞の増殖が悪くなるのです。そんなことが起きるとは思っていないため、原因が分からず、それを突き止めるのに苦労しました」と話します。
「また、シャーレも大型化し、多量に使用するので、インキュベーターに入れると、棚がたわんでしまうのです。そのため、細胞を均一に蒔いたつもりでも、培養するとシャーレ中の細胞密度が変わってしまう。棚がたわんでいるなどとは思わないので、原因発見には苦労しました」(松本さん)
長谷川さんは、「大きな突破口があったというよりも、こうした小さな改善の積み重ねこそが大きなカギとなっていきました。地道な積み重ねと細かい実験の繰り返しは、短期的には大きな成果に見えません。しかし、NEDOがそうした地道な努力を評価してくれたからこそ、今があります」と言います。
「研究は成果重視の世界なので、地道な研究に予算は付きにくいのですが、NEDOプロジェクトでは、地道な研究を評価してくれるのがありがたかったですね。学会発表では結果がしっかり出ていないといけないことが多いのですが、NEDOプロジェクトは短期間では成果が出ない、継続取得中のデータに対しても適切な評価をいただけました。研究者としては逆に新鮮で、実用化に向かうには、こうしたサポートが必要なのだと感じました」(長谷川さん)

写真3 gMSC®センターでは大量製造に向けた研究開発が続く
一方、岩本さんは、「NEDOのプロジェクトでの報告会を通して、実験方法を見直すことができました。私たちはベンチャーとして経験が浅いこともあり、NEDOのマネジメントによって、データの充実を図ることができました」と言います。
長谷川さんも報告会で、プロジェクト内の他グループの報告を聞けたことが役立ったと話します。「『ヒト幹細胞産業応用促進基盤技術開発』プロジェクトでは、機械工学的な知見も必要なのだということが分かり、タイムリーに情報共有できました」
こうしてツーセルは、プロトタイプ製剤を昇華させ、「gMSC®1」を臨床試験の段階に進めることができました。これは軟骨の再生を促す画期的な医療製品となることが期待されています。「gMSC®1」は、将来的には、一片の組織から理論上1,000〜1万人分の製剤が作製可能で、治療開始までの時間短縮や、大幅な治療費削減の実現が見込めます。
辻社長は、「長い時間がかかりましたが、ようやく軟骨の再生医療が現実になりつつあります。小さなベンチャーでは資金が続かなくて研究を進められないケースが多い中、当社は基礎研究から実用化まで続けることができ、支援をいただけたことをありがたいと思っています」と話します。
無重力状態で大量培養できる、画期的な装置「Gravite®」
再生医療の産業化を目指し結集した「ヒト幹細胞産業応用促進基盤技術開発」プロジェクトからは、「gMSC®1」の他に、「無重力下での大量培養技術」も開発されました。
「ヒト幹細胞産業応用促進基盤技術開発」が始まるときに、辻社長が参加を求めたのが、ツーセルと同じく広島大学発ベンチャー企業のスペース・バイオ・ラボラトリーズ(SBL)でした。
2005年に設立された同社は、広島大学の弓削類教授が開発した、重力環境を制御できる世界初の培養装置「Gravite®(グラビテ)」などの販売・開発活動を行っています。
もともと、ツーセルとSBLは、大学内の同じ建屋の中にあり、弓削教授と辻社長は親しい間柄でした。弓削教授は、「辻社長からは、MSCの大量培養に向けて、『Gravite®』を使えないかという話があり、NEDOプロジェクトに参加することになりました」と振り返ります。
「Gravite®」は、培養容器を二軸で回転することにより、360度全方位に重力を分散させ、中に入った試料にかかる重力を実質的に、1000分の1Gという微小重力(ほぼ無重力)から2〜3Gの過重力環境までを作り出すことができる画期的な装置です(写真4)。

写真4 Gravite®
プロジェクト参加以前から、弓削教授は微小重力下で幹細胞を培養すると、未分化性を維持したまま培養できること、さらには、微小重力で培養すると、天と地がなくなり、培養面積が大幅に増えるため、大量培養が可能になることを発見していました。
そこで弓削教授は、微小重力下で幹細胞を培養すれば、それを未分化状態のまま大量に培養でき、幹細胞の安定供給につながるとの着想のもと、「Gravite®」の開発を進めていました。しかし、NEDOプロジェクト参加以前の「Gravite®」には、培養装置としてはまだまだ改良すべき課題が残っていました。
そのためNEDOプロジェクトでは、ツーセルと共同で滑膜由来MSCの大量培養技術の開発を行い、「Gravite®」の改良を重ねていきました。
「Gravite®」は「gMSC®1」の完成に向けて、すぐにでも大きな威力を発揮すると予測されていましたが、培養容器と無血清培地の相性が良くありませんでした。「Gravite®」では、新たに開発された円筒形培養チューブに、折り畳んだフィルムを使用することで、大量培養を可能にしていました。しかし、無血清培地は培養容器表面の選り好みが大きく、一般的なフィルムでは、再現性をもって大量に培養することに難がありました。
SBL代表の河原裕美さんは、「通常のフィルム素材ではどうしても培養にムラができてしまい、その問題解決がなかなか困難でした」と話します。
「しかし、原因追及の経験は大きな財産になり、NEDOプロジェクト終了後も改良を重ね、ようやく昨年、無血清培地に合った高分子フィルムを発見して、培養が可能になりました」(河原さん)
「Gravite®」は2015年に販売を開始しました。最新バージョンでは、微小重力下では通常環境より約3倍速く増殖し、特別に開発した50mlの円筒形培養チューブを使うと、たった1本で直径10cmのシャーレ12枚分の培養面積を確保できます。

写真5 (左)微小重力環境を活かした大量培養を可能にする円筒形チューブ。(右)チューブ内のフィルム
この独創的な装置はアメリカのNASAでも高く評価され、2016年にNASAケネディ宇宙センターに導入され、動物や植物細胞、タンパク質結晶化など多くの研究者が「Gravite®」を使った研究を行っています。また、国際宇宙ステーションでの予備実験にも使われています。
「『Gravite®』の開発は、NEDOの支援がなければできなかったでしょう。現在も、広島大学でツーセルと一緒に共同研究を続けており、MSCの大量培養の研究にも、すでに取り組んでいます」(弓削教授)
FOR THE FUTURE 開発のいま、そして未来
製薬企業とライセンス契約し、患者のQOL向上を目指す
ツーセルでは、「gMSC®センター」での研究により、大量培養ができる体制が整いました。また、2016年4月には、「gMSC®1」に関する中外製薬とのライセンス契約が締結されました。その結果、ツーセルはいよいよ初回承認のための臨床試験の段階に進むことになりました。
ツーセルが行う臨床試験では、目標症例数を70症例と計画して、日本国内で膝関節の外傷性軟骨損傷および離断性骨軟骨炎の患者さんを募り、「gMSC®1」を移植した際の安全性や有効性を検討します。

写真6 「gMSC®1」のサンプル
中村教授は、「安全性を厳密に検証し、何が患者にとってメリットなのか評価しなければなりません。科学的なエビデンスを示して、患者さんの治療オプションを増やすことが大切です。新療法の有効性を実証できると期待しています」と言います。
「MSCの変形性膝関節症への将来の応用も重要です。人工関節も変形性関節症には優れた治療法ですが、痛みがなくなる反面、患者の活動性が落ち、スポーツなどはできなくなります。しかし、MSCによる再生治療を応用することが可能になれば、骨を切断するほど悪化する前に、早期治療を行って組織を温存し、患者さんのQOL(生活の質)向上に貢献できると考えています」(中村教授)
再生医療とリハビリロボットによるニューホスピタルに期待
一方、SBLでは、再生医療後の患者の運動機能を戻すためのリハビリテーション効果に着目して、「Gravite®」の将来像を探っています。
弓削教授は、「もともとリハビリテーションも専門の一つでした。そのため、早くから再生医療にはリハビリが必要だと気づいていました」と話します。
そのため、SBLでは「RE-Gait®(リゲイト)」という歩行支援ロボットも開発しています。運動障害や麻痺によって脚が不自由で歩行がうまくできない人のために足関節から歩行をアシストする装置です。
「RE-Gait®」は正常歩行がプログラムされているので、患者さんに合った歩行パターンを再学習させることができることから、「RE-Gait®」を外しても上手く歩くことができます。
「私は『Gravite®』を使った再生医療部門と『RE-Gait®』を使ったリハビリテーション部門を一つに融合した新しい病院構想『ニューホスピタル』を作りたいと思い、『Nature』誌に2017年に発表をしたところ、世界中から問合せがきました。以前は根治治療の再生医療にリハビリはいらないと言われたものですが、いまはその重要性が認識されるようになってきました」(弓削教授)
今後、弓削教授の語る再生医療とロボットによるリハビリを兼ね備えた病院が設立されれば、多くの患者の支えとなるでしょう。
開発者の横顔
再生医療が新しい産業になる
辻社長は、中外製薬株式会社で開発研究所安全センター長、メディカル事業部長を歴任しながら、再生医療の実用化を夢見てきました。
「20年間やってきて、ようやく再生医療が現実になります。加藤副社長と出会わなかったら、ツーセルも生まれていなかったでしょう。長い時間がかかりましたが、いよいよ再生医療が新しい産業になります」
辻社長は「これから臨床試験に全力で取り組む」と語ります。「多くの手間と費用がかかるでしょうが、それができる幸せをいま感じている」と言います。

株式会社ツーセル
代表取締役社長
辻 紘一郎 さん
リスクを恐れていては新しいものは生まれない
加藤副社長は、MSCと軟骨細胞の研究を長年続ける中で、アカデミックな研究とは別の社会貢献に必要性を感じたと言います。
「昔はアカデミックな研究者は産業のことを考えるなと言われたものです。しかし、研究を続けるうちに、日本の経済も調子が悪くなってきた。大学も日本のブレークスルーに寄与せよと言われるようになり、私の経験を産業に役立てようと決意しました。辻社長と出会って、こういう場にいることができたのは幸せです」
加藤副社長はかつて、ニューヨークに留学していたときに、「リスクを恐れていては新しいものは生まれない」と知ったと言います。「一般的に医薬品開発には事業リスクがありますが、必ず成し遂げたい」と力強く語ります。

株式会社ツーセル
取締役副社長
広島大学
名誉教授
加藤 幸夫 さん
軟骨損傷の患者さんを痛みから解放したい
自らもスポーツ好きの中村教授は、スポーツ整形外科やアスレティック・リハビリテーション分野で、研究と臨床を長らく続けてきました。
「軟骨を損傷したスポーツ選手が苦しむ姿を多く見てきました。十字靱帯を切って軟骨を痛めてしまったアメフト選手のひざを、やむを得ない選択とはいえ、手術し、引退させてしまったこともあります。軟骨の損傷が重症化すると、骨を切る手術をせざるを得なくなります。その前に軟骨の再生医療で悪化を止めて、患者さんを幸せにしたいと考えています」

大阪大学国際医工情報センター
招聘教授
中村 憲正 さん
NEDOプロジェクトを通してプレゼン能力が鍛えられました
大学では骨代謝の研究をしていた長谷川さんは、卒業後はベンチャー企業に入りたかったと言います。
「大学にいるときから、人と人との縁を取り持つことが好きでしたので、民間企業の方が力を発揮できると思ってツーセルに入社しました」
「当時は開発部といっても4、5人しか在籍していなかったこともあり、研究以外にも様々なプロジェクトに参加する機会をいただけました。そのお陰で、幅広い視点を身につけることができたと思います」
「NEDOプロジェクトでは社を代表してプレゼンテーションを行う機会をいただくなど、大勢の前での発表で鍛えられて度胸がつきました」

株式会社ツーセル 研究本部
副本部長/gMSC®センター長
長谷川 森一 さん
枠にとらわれず経験できる場所でした
大学時代から再生医療の産業化に関わりたいと思っていた岩本さんは、ツーセルで再生医療に携わっていこうと決意を新たにしたと言います。
「ツーセルはベンチャーで再生医療へ臨んでおり、多くの経験が積めると感じました。辻社長とも話をして、『長くツーセルに勤めている女性社員がいる』と聞き、実際に会ってみると人柄に惹かれ、一緒に働きたいと思ったのです。入社後は、想像以上に多くの経験を積める日々が待っていました」

株式会社ツーセル 研究本部
gMSC®センター副センター長
岩本 佳央梨 さん
リハビリを通じて再生医療の必要性を痛感
もともと広島大学で理学療法学を専攻していたという松本さんは、再生医療とリハビリの研究をしていたと言います。
「大学院でリハビリ中の患者さんと触れ合い、再生医療の必要性を当時から痛感していました。大学の研究室がツーセルとコラボレーションしており、長谷川さんと一緒に研究をしていました」
「弓削教授の『Gravite®』開発にも関わっていました。その流れで、弓削教授からツーセルを紹介していただき、辻社長にも誘っていただいたので入社しました。入社後は中村教授の元にも派遣され、研究をしました。NEDOプロジェクトで再生医療の事業化に向けた経験ができてよかったです」
今後は、リハビリの経験と知識も再生医療に活かしたいとのことです。

株式会社ツーセル
治験推進室副室長
松本 昌也 さん
アメリカ留学中に「Gravite®」のヒントを得る
弓削教授の専門の一つはリハビリテーション。アメリカ留学の際に米航空宇宙局(NASA)の研究者に研究指導を受けたことが「Gravite®」の開発につながったと言います。
「スポーツ医学で留学し、筋肉を増強する研究を行っていたときに、NASAの研究者から指導を受け、宇宙飛行士が宇宙空間では、筋肉や骨が委縮することから、無重力環境下では、筋肉や骨の分化、成熟が抑制されているのでは、と気づきました」
これをきっかけに「Gravite®」の開発につながり、資金繰りに苦労しながら作り上げました。
「Gravite®」で、MSCの未分化大量培養を行い、移植再生後にはリハビリができる、新しいタイプの病院を作ることが目標とのことです。

広島大学大学院
医歯薬保健学研究院教授
同大宇宙再生医療センター
センター長
株式会社スペース・バイオ・ラボラトリーズ
取締役
弓削 類 さん
患者さんを助けたい思いに変わりはない
広島大学薬学部から弓削教授の研究室に移ったという河原さんは、弓削教授に見込まれて、スペース・バイオ・ラボラトリーズの立ち上げと「Gravite®」開発に携わることになりました。
「広島大では教授がベンチャーを立ち上げて、研究室の学生が社長になることはよくあったので、違和感はありませんでした。むしろ、上司がいないので、社長業は楽しいですね」
「私はもともと栄養学を専攻し、その後、薬学部に移りましたが、『Gravite®』も『RE-Gait®』も健康科学という観点では同じなので、困っている患者さんを助けたいという思いに変わりはありません」

株式会社スペース・バイオ・ラボラトリーズ
代表取締役
広島大学宇宙再生医療センター
研究員
河原 裕美 さん
なるほど基礎知識
間葉系幹細胞の可能性と課題
「間葉系幹細胞(MSC=Mesenchymal Stem Cell)」とは、骨、軟骨、靱帯、筋肉、脂肪など中胚葉由来組織へ分化するのみならず、外胚葉および内胚葉由来組織(神経、肝臓など)へも分化する能力を持つ幹細胞です。
MSCは、成人の骨髄、脂肪、滑膜、歯髄など全身に幅広く存在し、容易に分離できます。また、MSCは培養条件を変えることで、骨、軟骨、脂肪に分化します。
弓削教授のグループが2013年に発表した研究では、脊髄損傷ラットモデルに「Gravite®」で培養したMSCを移植して、運動機能の回復を実現しました。また、同じくラットを使った実験で、肝機能や膵臓の治療効果も確認されており、今後、MSC再生医療は大きな可能性を持っています。
ただし、ツーセルの研究者や中村教授たちの論文(『幹細胞用無血清培地の開発』)によれば、「MSC移植療法には多くの臨床例(骨疾患、関節疾患、心疾患、脳梗塞、骨髄移植での移植片対宿主病)があります。しかし、臨床成績は必ずしも一定しない。多くの臨床研究の中には、有効性を統計的に証明できなかったものもあるようです。臨床研究で有効性を証明するためには、できるだけ高品質のMSCを使用するべきである」と述べられています。
今回の「gMSC®1」の開発の意義は、こうした点にもあると考えられます。
NEDOの役割
「再生医療評価研究開発事業/三次元複合臓器構造体研究開発」
(2006−2009年度)
再生医療への期待が社会的に高まる中、NEDOではこれまで、再生医療の産業化を目指したプロジェクトを実施してきました。
今回の滑膜由来間葉系幹細胞を対象とした研究開発では、無血清培地や培養基盤技術の開発といった基盤技術開発から、スケールアップや製剤化技術の開発などの応用技術開発まで、実用化に向けてシームレスな支援を行いました。
その中でのマネジメントとして、例えば「ヒト幹細胞産業応用促進基盤技術開発」では、産学官のプレイヤーの連携促進に向けた取り組みを実施しました。実施者以外の有識者からなる運営会議を設置し、プロジェクトに対する提言収集の場を設けるなど、最大限の研究開発成果が得られる仕組みを作りました。また、グループ内での連絡会等を定期的に開催し、産学官連携のもと効率的に研究開発を推進しました。これらの取り組みにより、将来の再生医療の発展の礎となる技術の開発に貢献しました。
関連プロジェクト
お読みいただきありがとうございました。
ぜひともアンケートにお答えいただき、
お読みいただいた感想をお聞かせください。
いただいた感想は、
今後の連載の参考とさせていただきます。



